Kierownik projektu
:
mgr Łukasz Suprewicz
Uniwersytet Medyczny w Białymstoku
Panel: NZ6
Konkurs
: PRELUDIUM 21
ogłoszony
28 marca 2022 r.
Wirus SARS-CoV-2, odpowiedzialny za wybuch pandemii COVID-19 w 2020 roku, wywarł ogromny wpływ na światowe systemy ochrony zdrowia. Początkowo uważany był za czynnik zakażeń układu oddechowego, ale okazało się, że jest także przyczyną poważnych uszkodzeń ośrodkowego układu nerwowego (OUN). Aż 40% zakażonych pacjentów doświadcza przewlekłych objawów neurologicznych, popularnie nazywanych „mgłą covidową”. Chociaż niektóre z tych objawów, (np. zawroty głowy) są stosunkowo łagodne, to u niektórych pacjentów dochodzi do poważnych następstw, takich jak udar czy encefalopatia (uszkodzenie mózgowia). Wobec ciągle toczącej się pandemii SARS-CoV-2, kluczowe jest zrozumienie mechanizmu tych uszkodzeń i opracowanie skutecznych metod ich leczenia.
 Łukasz Suprewicz, fot. Michał Łepecki
Łukasz Suprewicz, fot. Michał Łepecki
Sposób, w jaki SARS-CoV-2 wpływa na mózg pozostaje nadal przedmiotem intensywnych badań. Jedna z hipotez mówi o nadmiernym wydzielaniu mediatorów zapalnych, określanym jako „burza cytokinowa”, oraz o bezpośrednim wpływie białka S, które wirus wykorzystuje do wniknięcia do naszych komórek. Te procesy są łączone z uszkodzeniem bariery między krwią a strukturami mózgu (tzw. bariery krew-mózg). Jej przerwanie prowadzi do zwiększonego przenikania do mózgu szkodliwych substancji, m.in. wirusów i czynników zapalnych.
W tym kontekście pojawia się rola wimentyny ‒ białka, które buduje cytoszkielet większości komórek, gdzie odgrywa kluczową rolę w procesach takich jak podział komórkowy, migracja oraz ochrona jądra komórkowego przed uszkodzeniem mechanicznym. Wimentyna może być wydzielana do krwi przez komórki układu immunologicznego w odpowiedzi na stan zapalny i nazywamy ją wówczas wimentyną zewnątrzkomórkową. Wyróżniamy dwie formy zewnątrzkomórkowej wimentyny: związaną z powierzchnią komórki oraz niezwiązaną. W jednej z wcześniejszych prac wykazaliśmy, że zewnątrzkomórkowa wimentyna pełni rolę koreceptora dla SARS-CoV-2, a więc jest niezbędna do skutecznej infekcji komórek (Suprewicz et. al. Small 2022).
 Łukasz Suprewicz, fot. Michał Łepecki
Celem projektu jest poznanie roli zewnątrzkomórkowej wimentyny w procesie zapalnym w OUN towarzyszącym zakażeniu SARS-CoV-2. Badamy mechanizm wpływu zewnątrzkomórkowej wimentyny na różne rodzaje komórek występujących w obrębie mózgu, takich jak komórki śródbłonka i astrocyty. Wykorzystujemy trójwymiarowy model bariery krew-mózg w przepływie, aby ocenić przepuszczalność i integralność komórek śródbłonka, a także adhezję i migrację komórek immunologicznych w obecności wimentyny oraz białka SARS-CoV-2. W kolejnym etapie badań ocenimy wpływ badanych substancji na stan zapalny poprzez analizę wydzielania mediatorów zapalnych. Ostatecznie, na poziomie molekularnym, zbadane zostaną szlaki sygnałowe charakterystyczne dla infekcji SARS-CoV-2 oraz uszkodzenia naczyń krwionośnych.
Łukasz Suprewicz, fot. Michał Łepecki
Celem projektu jest poznanie roli zewnątrzkomórkowej wimentyny w procesie zapalnym w OUN towarzyszącym zakażeniu SARS-CoV-2. Badamy mechanizm wpływu zewnątrzkomórkowej wimentyny na różne rodzaje komórek występujących w obrębie mózgu, takich jak komórki śródbłonka i astrocyty. Wykorzystujemy trójwymiarowy model bariery krew-mózg w przepływie, aby ocenić przepuszczalność i integralność komórek śródbłonka, a także adhezję i migrację komórek immunologicznych w obecności wimentyny oraz białka SARS-CoV-2. W kolejnym etapie badań ocenimy wpływ badanych substancji na stan zapalny poprzez analizę wydzielania mediatorów zapalnych. Ostatecznie, na poziomie molekularnym, zbadane zostaną szlaki sygnałowe charakterystyczne dla infekcji SARS-CoV-2 oraz uszkodzenia naczyń krwionośnych.
Wyniki uzyskane w ramach tego projektu mogą znacząco rozszerzyć naszą wiedzę na temat wpływu zewnątrzkomórkowej wimentyny i jej modyfikacji na interakcję komórek śródbłonka i komórek immunologicznych podczas zakażenia SARS-CoV-2. To może przyczynić się do skuteczniejszego leczenia pacjentów z COVID-19, w szczególności tych, którzy doświadczają powikłań neurologicznych. Praca może także wskazać nowe cele terapeutyczne, które pomogą w walce z ewentualnymi, kolejnymi globalnymi pandemiami, biorąc pod uwagę, że rola zewnątrzkomórkowej wimentyny jako koreceptora nie jest ograniczona jedynie do SARS-CoV-2 lecz dotyczy również innych zakażeń, w tym bakteryjnych.
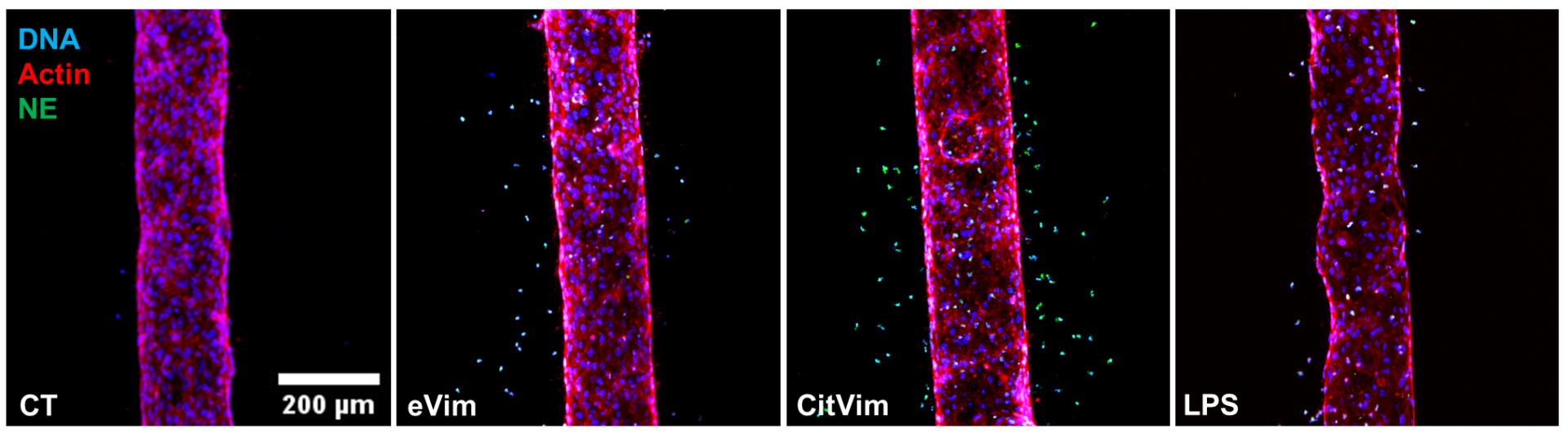
Diapedeza ludzkich neutrofilów nietraktowanych lub stymulowanych wimentyną (Vim), cytrulinowaną wimentyną (CitVim) lub lipopolisacharydem (LPS) w model 3D naczyń krwionośnych. Elastaza neutrofilowa (zielony), aktyna (czerwony), DNA (niebieski).
Pełny tytuł finansowanego projektu: Zewnątrzkomórkowa wimentyna jako cząsteczka sygnałowa w patogenezie zapalenia i uszkodzenia centralnego układu nerwowego u pacjentów z COVID-19
mgr Łukasz Suprewicz
Absolwent Uniwersytetu Medycznego w Białymstoku, diagnosta laboratoryjny. Student IV roku Szkoły Doktorskiej UMB. Autor i współautor ponad dwudziestu publikacji w czasopismach międzynarodowych. W badaniach koncentruje się na poznaniu mechanizmów molekularnych interakcji pomiędzy białkami, patogenami, a komórkami odpowiedzi immunologicznej. Poza kierowaniem projektem PRELUDIUM 21 bierze udział w realizacji grantu PRELUDIUM BIS 1, którego kierownikiem jest prof. dr hab. Robert Bucki.